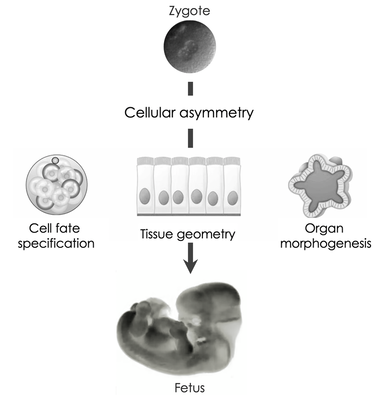
私達のカラダの中にある細胞は、もとはたった一つの細胞「受精卵」からつくられます。受精卵とは、卵母細胞と精子が融合してつくられる特殊な細胞で、どのような細胞種にも分化できる「全能性」を保持しています。受精卵が分裂してつくり出す細胞はその後、体細胞と生殖細胞に分化していきます。体細胞はカラダの組織・器官を構成し、生殖細胞は遺伝情報を次世代へと継承するための卵母細胞と精子をつくりだします。それぞれの細胞がどの細胞種へ分化するのかという「細胞の運命を決める仕組み」には、未だに多くの謎が残されています。
The development of multi-cellular organisms begins from a single-celled zygote. A zygote is created through the fusion of an oocyte with sperm, at which point it acquires “totipotency”, allowing it to produce all the differentiated cells of the body and organize them in a specific spatial and temporal sequence. During development, the zygote will generate two cell types somatic cells, which constitute all of an organism’s body cells, and germ cells, which give rise to gametes (egg and sperm). How the fate of cells is defined, and how the spatio-temporal dynamics of fate specification are programmed during development, remains one of the biggest mysteries in biology.
The development of multi-cellular organisms begins from a single-celled zygote. A zygote is created through the fusion of an oocyte with sperm, at which point it acquires “totipotency”, allowing it to produce all the differentiated cells of the body and organize them in a specific spatial and temporal sequence. During development, the zygote will generate two cell types somatic cells, which constitute all of an organism’s body cells, and germ cells, which give rise to gametes (egg and sperm). How the fate of cells is defined, and how the spatio-temporal dynamics of fate specification are programmed during development, remains one of the biggest mysteries in biology.
これまでの研究から、受精卵には細胞の運命を決める「運命決定因子」が存在していると提唱されています。細胞内でこの「運命決定因子」の濃度または活性状態の分布が均一であれば、細胞分裂後の娘細胞は同じ細胞運命を辿りますが、分布が非対称であれば、二つの娘細胞はそれぞれ別々の運命を歩みます(図1)。このような、因子の細胞内空間分布を利用した細胞運命決定は、受精卵のみならず様々な細胞種で活用されています。例えば成体にある組織幹細胞は、細胞分裂を介して幹細胞と分化細胞をつくることで組織の恒常性維持にはたらきますが、この幹細胞―分化細胞の運命決定には「運命決定因子」の細胞内分布パターンが重要であると提唱されています。
Previous studies discovered that “fate determinants” that are essential for cell fate specification during development. These proteins often exhibit an asymmetric pattern of intracellular distribution and are inherited into one of the two daughter cells during cell division, suggesting that the fate of cells depends on the intrinsic concentration and/or activity of the determinants. This concept of cell fate determination can be applied to many types of cells, including somatic stem cells. Somatic stem cells are capable of self-renewing, as well as giving rise to differentiated cells. The balance between self-renewal and differentiation relies on the intrinsic properties of the fate determinants.
Previous studies discovered that “fate determinants” that are essential for cell fate specification during development. These proteins often exhibit an asymmetric pattern of intracellular distribution and are inherited into one of the two daughter cells during cell division, suggesting that the fate of cells depends on the intrinsic concentration and/or activity of the determinants. This concept of cell fate determination can be applied to many types of cells, including somatic stem cells. Somatic stem cells are capable of self-renewing, as well as giving rise to differentiated cells. The balance between self-renewal and differentiation relies on the intrinsic properties of the fate determinants.
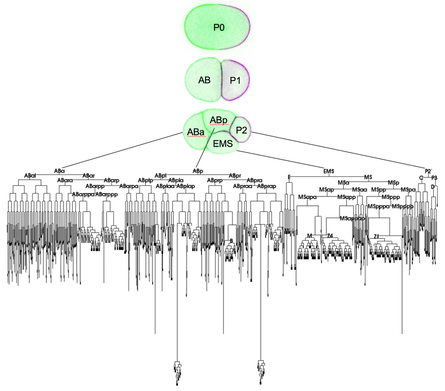
それでは運命決定因子の細胞内の空間パターンはどのように決まるのでしょうか?線虫C. elegansの受精卵を調べた研究から、これにはPAR (partitioning-defective)と呼ばれる6種類の遺伝子が関わることが明らかになりました。線虫の受精卵もヒトと同じように、細胞分裂を介して体細胞と生殖細胞を作りますが、PAR遺伝子が欠損した受精卵ではこの運命決定が起こりません。受精卵においてPAR遺伝子産物がどこに局在するか調べたところ、4種類のPAR遺伝子産物は将来の体細胞側に、2種類のPAR遺伝子産物は将来の生殖細胞側に配向していることがわかりました。すなわちPAR遺伝子産物は、自身が細胞内で非対称化することで、運命決定因子の空間パターンを調節していると示唆されます(図2)。
These studies raised a fundamental question: How is the spatial information of the cell patterned? In other words, how is genetic information translated in a reliable manner to give rise to a specific, stereotyped pattern in differentiated cells? A hint came from genetic studies using the nematode Caenorhabditis elegans, where it was discovered that a set of six partitioning-defective (par) genes acted as essential maternal factors for fate specification of the somatic and germ cells during embryogenesis. Notably, the PAR gene products exhibit asymmetric patterns in zygotes: four proteins are enriched at the cell cortex, close to future somatic cells, and the others are seen at the cortex, near the future germ cells.
These studies raised a fundamental question: How is the spatial information of the cell patterned? In other words, how is genetic information translated in a reliable manner to give rise to a specific, stereotyped pattern in differentiated cells? A hint came from genetic studies using the nematode Caenorhabditis elegans, where it was discovered that a set of six partitioning-defective (par) genes acted as essential maternal factors for fate specification of the somatic and germ cells during embryogenesis. Notably, the PAR gene products exhibit asymmetric patterns in zygotes: four proteins are enriched at the cell cortex, close to future somatic cells, and the others are seen at the cortex, near the future germ cells.
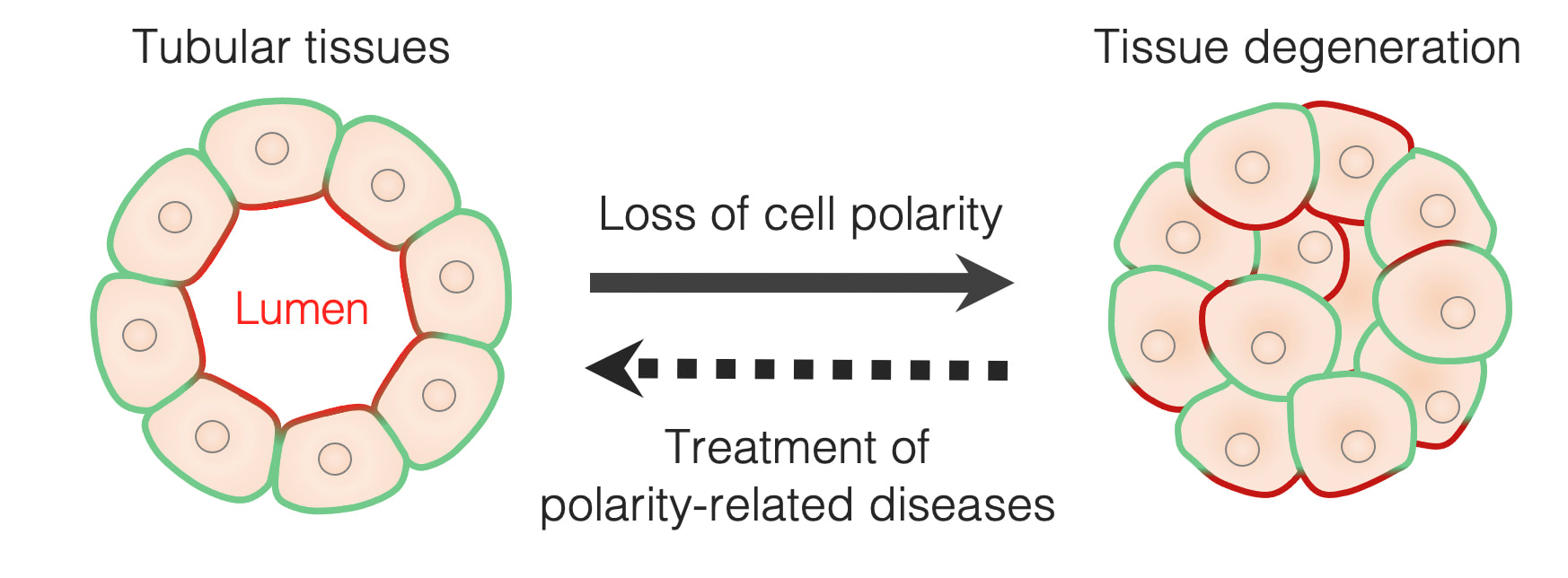
この線虫から同定されたPAR遺伝子は様々な生物種で保存されており、多様な細胞種における空間パターンを決める鍵となる「細胞内極性のマスター制御因子」であることがわかってきました。またヒトでは、PAR遺伝子に変異を有すると、癌化・神経変性・幹細胞の不足による老化の促進などが起こることから、「PARによる正常な細胞極性の形成と維持が、様々な疾患の発症を抑制する」と提唱されています。すなわち、細胞内の空間パターンを制御する細胞極性のメカニズムを深く理解し、細胞極性を人為的に制御することができれば、ヒトにおける様々な疾患発症の予防策を考える礎となると期待されます。
Now, PAR proteins are considered to be the key regulators of intracellular spatial information. PAR proteins are highly conserved among metazoans, and are involved in the establishment of cell asymmetry in many cell types during development. Several studies have also demonstrated that inhibition of PAR function induces tumorigenesis in many tissues, neurodegeneration, and premature aging due to a loss of somatic stem cells, indicating a role for PAR-dependent cell asymmetry in protecting adults from these diseases. Therefore, a holistic understanding of the mechanisms underlying cellular asymmetry will be vital for developing precision medicine for the prevention and treatment of human diseases.
Now, PAR proteins are considered to be the key regulators of intracellular spatial information. PAR proteins are highly conserved among metazoans, and are involved in the establishment of cell asymmetry in many cell types during development. Several studies have also demonstrated that inhibition of PAR function induces tumorigenesis in many tissues, neurodegeneration, and premature aging due to a loss of somatic stem cells, indicating a role for PAR-dependent cell asymmetry in protecting adults from these diseases. Therefore, a holistic understanding of the mechanisms underlying cellular asymmetry will be vital for developing precision medicine for the prevention and treatment of human diseases.
PAR遺伝子の生体内における役割がわかってきた一方、細胞極性のメカニズムには未だに多くの謎が隠されています。PAR遺伝子産物はどのように非対称パターンを獲得するのか? PAR遺伝子産物はどのように体細胞と生殖細胞の運命を決めるのか? PAR遺伝子は上皮細胞や神経細胞など形態が異なる分化細胞においても同じ働きをしているのか?老化による生体組織の破綻と細胞極性の異常は密接に関係しているが、老化とPAR遺伝子機能には直接の因果関係があるのか?私達はこれらの疑問に答えていくことで、「細胞内の空間パターンを司る仕組み」の本質に迫り、更に細胞極性異常が引き起こす先天性疾患に対して、医学的アプローチを見いだすことができると考えています。
A major challenge in cell-developmental biology is developing a comprehensive model that encompasses the full complexity of the spatio-temporal modulation of these cell polarity regulators. How is the patterning of PAR proteins encoded in the genome? How can the pattern of PAR proteins specify the binary choice between somatic and germ cell fate? How can the same set of PAR proteins facilitate the interior organization of many different types of differentiated cells? How does the PAR polarity system break down during aging? Research addressing these questions will shed light on the fundamental principles of cell physiology and reveal how these principles might govern the progression of disease and the response of disease to intervention.
A major challenge in cell-developmental biology is developing a comprehensive model that encompasses the full complexity of the spatio-temporal modulation of these cell polarity regulators. How is the patterning of PAR proteins encoded in the genome? How can the pattern of PAR proteins specify the binary choice between somatic and germ cell fate? How can the same set of PAR proteins facilitate the interior organization of many different types of differentiated cells? How does the PAR polarity system break down during aging? Research addressing these questions will shed light on the fundamental principles of cell physiology and reveal how these principles might govern the progression of disease and the response of disease to intervention.
私達の研究グループでは、細胞極性の分子メカニズムを体系的に理解するために、遺伝学を用いた新規の細胞極性因子同定、光遺伝学・温度遺伝学を駆使した標的因子の細胞内機能の解析を進めています。さらに、高速・高解像度のライブイメージングにより、「コンピュータ駆動型画像解析」を用いて分子・細胞・組織の動態を定量的に記述することで、種々の細胞が空間パターンを調節するダイナミクスを分子レベルで明らかにしていきます。私達はこれらの研究を通して、細胞生物学・発生生物学・分子生物学にコンピュータサイエンス・細胞組織工学・医学の視点を融合させた新しい研究領域を確立することを目指します。
Our group aims to understand the chemical and mechanical control of cell polarity, from which complex cell and tissue functions are built across different biological scales. With insights from our research, we hope to develop new concepts for understanding how normal development is ensured, and how it can be compromised in disease and aging. To do this, we will develop new technologies for high-resolution live-cell imaging, computer-assisted quantitative data analysis, and genetic approaches by which cell asymmetry can be manipulated in living organisms. Our laboratory serves as a vibrant platform for post-graduate research training by establishing an inter-disciplinary research environment that incorporates diverse fields of science and engineering. We welcome enthusiastic students and junior scientists in science, engineering, physiology, and computer science to join us at Hokkaido University.
Our group aims to understand the chemical and mechanical control of cell polarity, from which complex cell and tissue functions are built across different biological scales. With insights from our research, we hope to develop new concepts for understanding how normal development is ensured, and how it can be compromised in disease and aging. To do this, we will develop new technologies for high-resolution live-cell imaging, computer-assisted quantitative data analysis, and genetic approaches by which cell asymmetry can be manipulated in living organisms. Our laboratory serves as a vibrant platform for post-graduate research training by establishing an inter-disciplinary research environment that incorporates diverse fields of science and engineering. We welcome enthusiastic students and junior scientists in science, engineering, physiology, and computer science to join us at Hokkaido University.
Proudly powered by Weebly