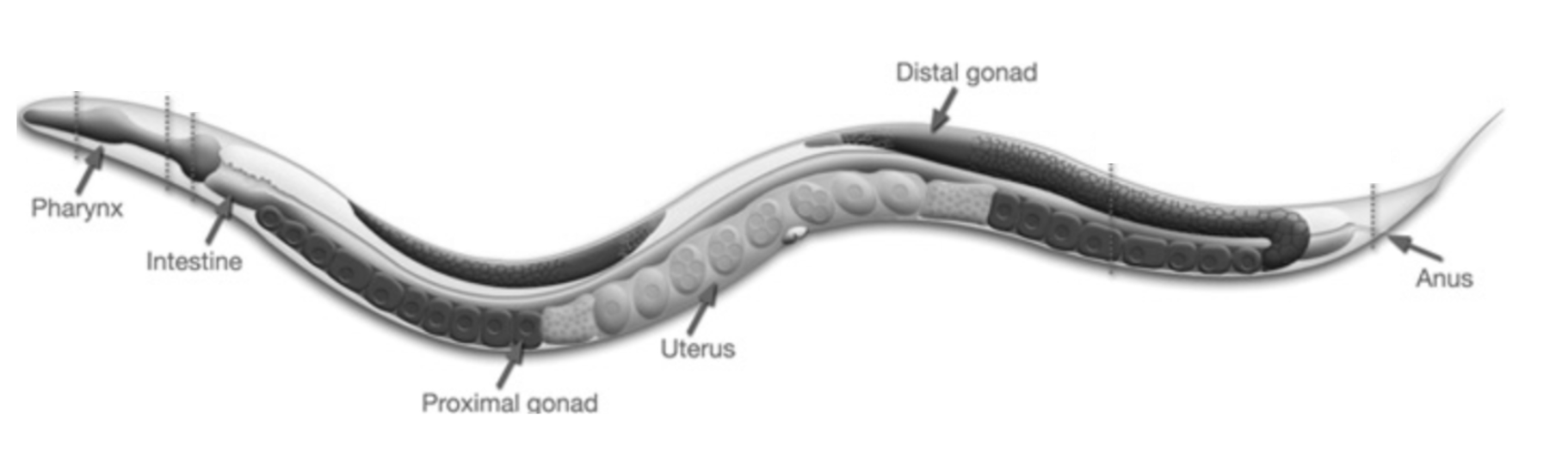
線虫C. elegansは、体長約1mmの透明な体をした多細胞生物で、そのカラダは約1000個の細胞から構成されています。受精卵が様々な細胞種と組織をつくりだす過程を「発生」と呼びますが、線虫は発生における細胞分裂・運命決定の時空間パターンがとても厳密に制御されています。つまりどの個体においても、それぞれの細胞が「同じ時期に同じ場所で」細胞分裂と運命決定を行います。従って、発生における遺伝子発現やタンパク質の生成・分解・ダイナミクスを定量的に調べるには、最も優れたモデル動物であると言えます。
Caenorhabditis elegans (C. elegans) is a free-living transparent nematode about 1 mm in length in adults. This animal is composed of about 1,000 cells, which are created through stereotyped cell lineage, with reproducible patterns of cell divisions and fate specifications throughout development. The invariant cell lineage provides a unique opportunity to decode the molecular mechanisms of animal development by describing the behavior of molecules and cells in a quantitative manner.
Caenorhabditis elegans (C. elegans) is a free-living transparent nematode about 1 mm in length in adults. This animal is composed of about 1,000 cells, which are created through stereotyped cell lineage, with reproducible patterns of cell divisions and fate specifications throughout development. The invariant cell lineage provides a unique opportunity to decode the molecular mechanisms of animal development by describing the behavior of molecules and cells in a quantitative manner.
線虫の受精卵は、卵母細胞と精子が融合した直後には細胞内の分子に空間的な偏りを示しませんが、受精後20分経過すると様々な分子が非対称パターンを示し始めます。この非対称化が細胞分裂の前に起こることによって、受精卵に存在する運命決定因子が二つの娘細胞へ非対称に分配され、体細胞と生殖細胞という異なる細胞運命を生み出します。受精卵が「対称から非対称」に転換する仕組みは長らく不明のままでしたが、私達の研究グループはその仕組みに具体的なメカニズムを提唱してきました。
The newly fertilized C. elegans zygote is one of the best-studied systems for the establishment of cell polarity. The zygote is initially unpolarized, but begins the polarization process by rearranging intracellular molecules and organelles in a spatially biased manner. The resultant asymmetries in the zygote mediate unequal inheritance of cell fate determinants to the anterior blastomere, which gives rise to somatic cells, and the posterior blastomere, which produces the germ cells. Our group studies the mechanisms that ensure this asymmetric mode of cell division and facilitate the dichotomy of germ-soma cell fate in the zygote.
The newly fertilized C. elegans zygote is one of the best-studied systems for the establishment of cell polarity. The zygote is initially unpolarized, but begins the polarization process by rearranging intracellular molecules and organelles in a spatially biased manner. The resultant asymmetries in the zygote mediate unequal inheritance of cell fate determinants to the anterior blastomere, which gives rise to somatic cells, and the posterior blastomere, which produces the germ cells. Our group studies the mechanisms that ensure this asymmetric mode of cell division and facilitate the dichotomy of germ-soma cell fate in the zygote.
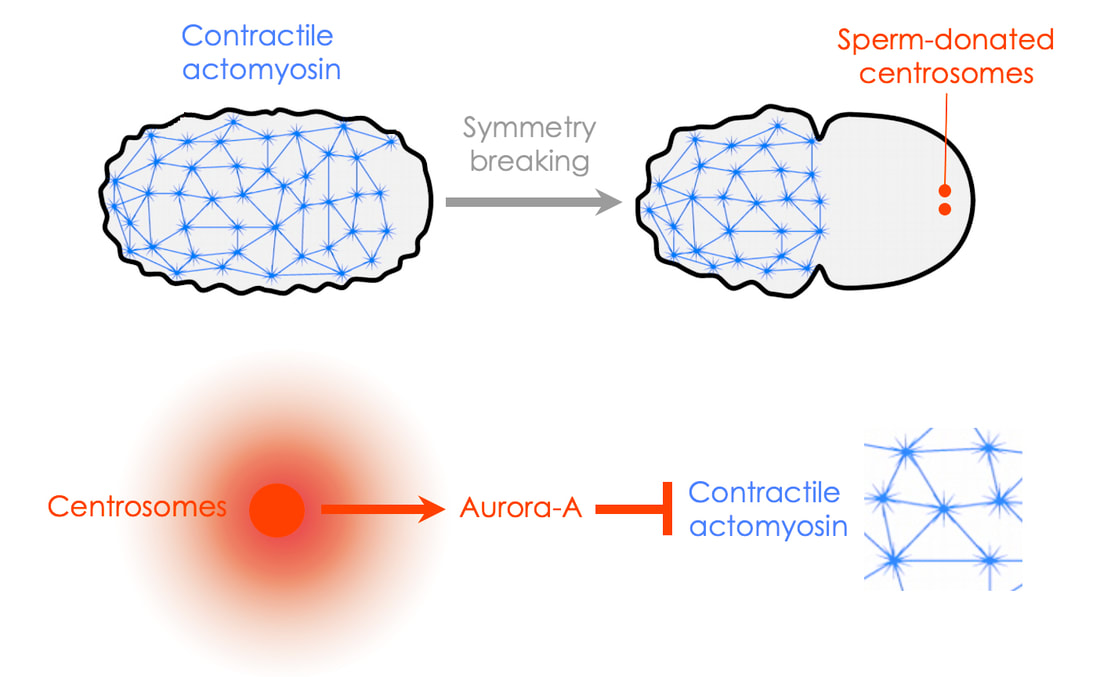
受精卵で起こる様々な分子の非対称化には、精子由来の中心体が必要であることが報告されています。受精時に精子により持ちこまれる中心体は細胞の片側に局在し、この場所から極性化が始まることから、この構造が非対称化の引き金を引くと考えられていましたが、その分子実態は明らかになっていませんでした。これまでに私達は、中心子周辺物質(PCM)成分の一つであるAurora-Aキナーゼが、受精卵の非対称化に必要かつ十分であることを明らかにしました(ref)。受精卵においてAurora-Aキナーゼは中心子により活性化され、この活性化型Aurora-Aキナーゼは細胞膜近傍に存在しているアクチン骨格構造を局所的に阻害します。このAurora-Aによる細胞骨格の阻害が、前述のPAR遺伝子産物の局在の非対称化を引き起こします。
How does the zygote initiate polarization? Genetic evidence suggests that the sperm-donated centrosome acts as a spatial cue that breaks the symmetry in the zygote. The centrosome is an organelle that is composed of a pair of centrioles surrounded by pericentriolar material (PCM). The identity of the key molecule that links the centrosome to cell polarity was previously a mystery for over 20 years. We identified one of the PCM components, Aurora-A kinase, as the long sought-after “symmetry-breaking cue”. This kinase is activated by the PCM, and then diffuses toward the cell cortex proximal to the centrosome, where the active kinase locally interferes with the cortical actomyosin network.
How does the zygote initiate polarization? Genetic evidence suggests that the sperm-donated centrosome acts as a spatial cue that breaks the symmetry in the zygote. The centrosome is an organelle that is composed of a pair of centrioles surrounded by pericentriolar material (PCM). The identity of the key molecule that links the centrosome to cell polarity was previously a mystery for over 20 years. We identified one of the PCM components, Aurora-A kinase, as the long sought-after “symmetry-breaking cue”. This kinase is activated by the PCM, and then diffuses toward the cell cortex proximal to the centrosome, where the active kinase locally interferes with the cortical actomyosin network.
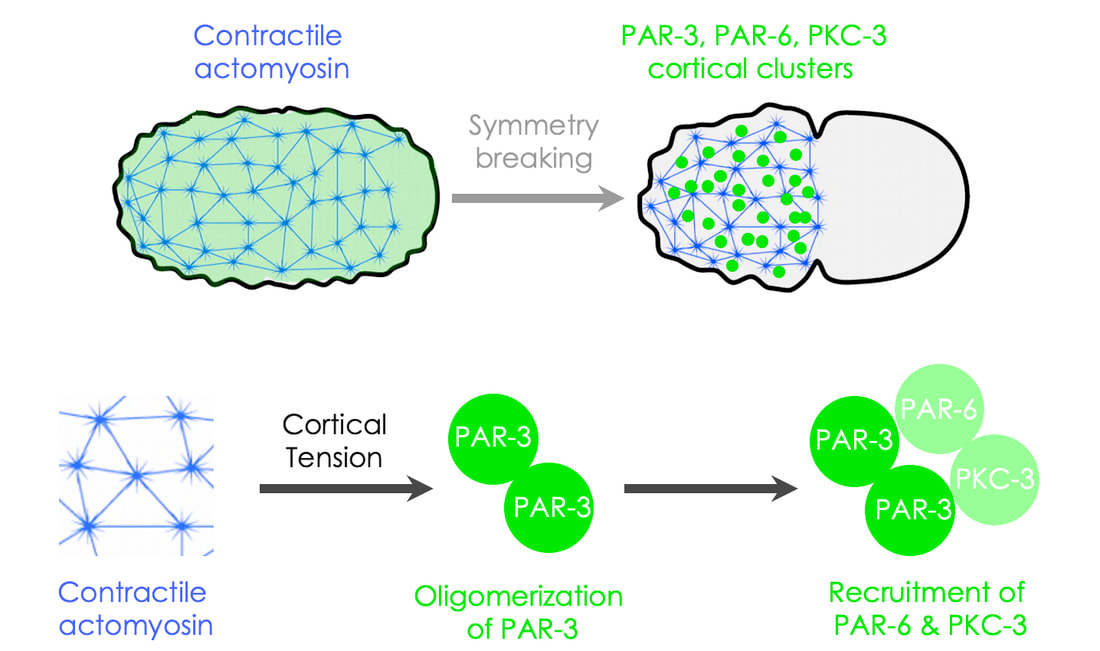
アクチン骨格とは、アクチン繊維にモータータンパク質ミオシンが結合した構造体であり、この構造が筋肉のように収縮することで、細胞膜近傍に力刺激を及ぼします。Aurora-Aがアクチン骨格を局所的に阻害することで、細胞膜にかかる力刺激には「非対称性」が生じます。私達は、この力刺激の非対称性がPAR遺伝子産物の細胞内分布を変化させる仕組みを明らかにしました(ref)。PAR遺伝子産物の一つPAR-3タンパク質は細胞膜にかかる収縮力(張力?)を感知し、細胞膜上で凝集体を形成します。さらに、細胞内の非対称なアクトミオシン構造の分布と収縮が、細胞膜上のPAR-3凝集体を中心体Aurora-Aとは反対の方向へ輸送します。これらの仕組みが協働することで、PAR-3は細胞膜における非対称パターンを獲得します(図6)。
The local disruption of the cortical actomyosin network generates unbalanced mechanical cortical forces, which ultimately trigger advective flows of cortical proteins away from the centrosome. This creates unbalanced hydrodynamic forces within the cortex, which consequently flows as a viscous material. This flow enhances the stabilization of cortical PAR proteins, leading to their passive transport by the cortical flows. Cortical contractility, and the resulting increase in cortical tension, is essential for PAR-‐3 to form cortical clusters, retard cortical turnover, and co-‐migrate with cortical actomyosin. Therefore, two types of cortical mechanics (advective flows and cortical tension) synergistically stimulate the efficient segregation of the cortical PAR-3 complex to the anteriorcompartment.
The local disruption of the cortical actomyosin network generates unbalanced mechanical cortical forces, which ultimately trigger advective flows of cortical proteins away from the centrosome. This creates unbalanced hydrodynamic forces within the cortex, which consequently flows as a viscous material. This flow enhances the stabilization of cortical PAR proteins, leading to their passive transport by the cortical flows. Cortical contractility, and the resulting increase in cortical tension, is essential for PAR-‐3 to form cortical clusters, retard cortical turnover, and co-‐migrate with cortical actomyosin. Therefore, two types of cortical mechanics (advective flows and cortical tension) synergistically stimulate the efficient segregation of the cortical PAR-3 complex to the anteriorcompartment.
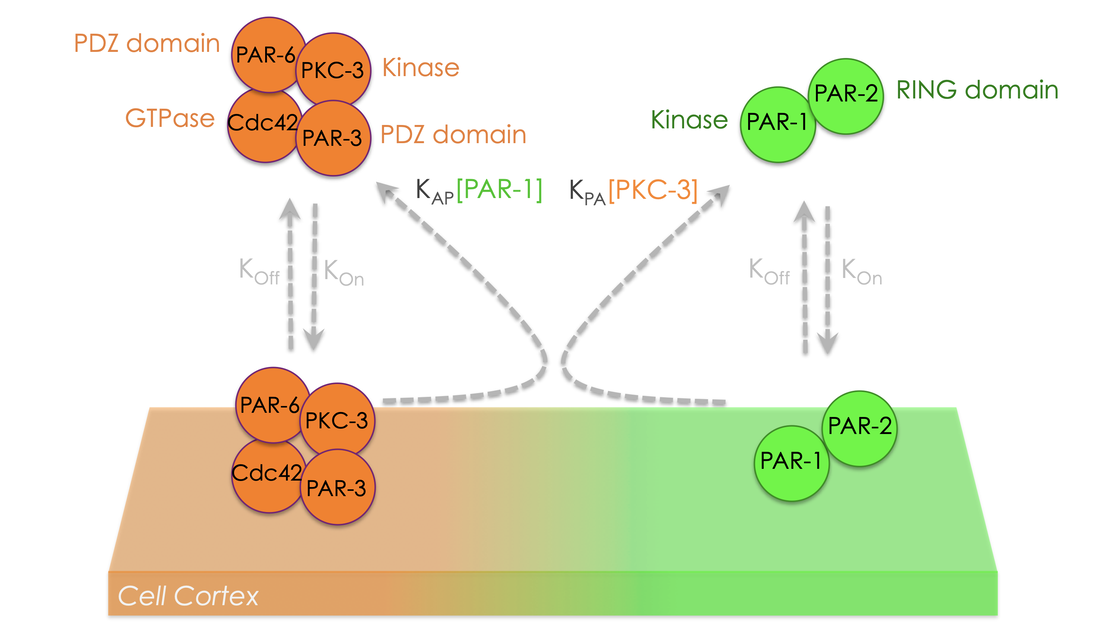
さらに我々は、細胞膜上でPAR-3の凝集構造がaPKCキナーゼの集積を誘導することを明らかにしました。また、aPKCの標的としてPAR遺伝子産物のPAR-1とPAR-2を同定し、これらの相互作用を明らかにしました。PAR-1とPAR-2は複合体を形成する脂質結合タンパク質であり、両者の膜結合はaPKCによるリン酸化によって阻害されることがわかりました。つまり、細胞膜上にPAR-3―aPKC複合体が存在すると、PAR-1―PAR-2はその場所には同時に局在できないことになります。さらに、細胞膜に集積したPAR-1キナーゼは、PAR-3をリン酸化して細胞膜から排除することも分かりました。すなわち、PAR-3―aPKC複合体とPAR-1―PAR-2複合体は「相互に排他的な関係」を築くことで、細胞膜で互いに重なり合わない非対称パターンを獲得します(図7)。
Asymmetric enrichment of cortical PAR-3 clusters leads to accumulation of aPKC kinase at the anterior cortex. We uncovered that aPKC directly targets two PAR proteins, PAR-1 and PAR-2. Both PAR-1 and PAR-2 are capable of binding to plasma membrane phospholipids, which can be inhibited via direct phosphorylation by aPKC. Thus, the PAR-3-aPKC complex excludes PAR-1 and PAR-2 from the anterior cortex, allowing them to form a posterior-enriched cortical gradient. PAR-1 in turn phosphorylates and excludes PAR-3 from the posterior cortex. This multilayered feedback between chemical signaling and mechanical regulation support the robust and stereotypical nature of cortical polarization.
Asymmetric enrichment of cortical PAR-3 clusters leads to accumulation of aPKC kinase at the anterior cortex. We uncovered that aPKC directly targets two PAR proteins, PAR-1 and PAR-2. Both PAR-1 and PAR-2 are capable of binding to plasma membrane phospholipids, which can be inhibited via direct phosphorylation by aPKC. Thus, the PAR-3-aPKC complex excludes PAR-1 and PAR-2 from the anterior cortex, allowing them to form a posterior-enriched cortical gradient. PAR-1 in turn phosphorylates and excludes PAR-3 from the posterior cortex. This multilayered feedback between chemical signaling and mechanical regulation support the robust and stereotypical nature of cortical polarization.
中心体による細胞極性の誘導・PAR複合体の非対称パターニング・PAR複合体による細胞運命決定などの分子メカニズム、が明らかになってきたのは、ここ10年程度の研究成果によるものです。近年の生細胞高解像度イメージング技術の向上や、光遺伝学等の遺伝子機能操作技術の開発によって、今後も細胞極性の研究は飛躍的に進んでいくと期待されます。私達の研究グループは、線虫と哺乳動物培養細胞を併用し、受精卵・生殖細胞前駆体・腸細胞前駆体・上皮細胞などの極性化を理解することを通して、細胞極性を司る普遍的な分子メカニズムを明らかにしていきます。また個体発生を通して、細胞極性と組織恒常性・老化をリンクする接点を探索していきます。
Many discoveries in the regulation of cell polarity have been made in only the last 10 years. Recent developments in state-of-the-art live-cell imaging (e.g., high-speed super-resolution microscopy) and genetic approaches that can manipulate gene functions in vivo (e.g., opto-genetics) have enabled scientists to delve into the chemical and mechanical control of biological asymmetry across different scales, from molecules, to cells, to tissues, to organisms. By taking an inter-disciplinary approach that harnesses recent technologies from diverse fields of science and engineering, our laboratory will continue to pursue cutting-edge science and build a network with leading scientists in cell and developmental biology.
Many discoveries in the regulation of cell polarity have been made in only the last 10 years. Recent developments in state-of-the-art live-cell imaging (e.g., high-speed super-resolution microscopy) and genetic approaches that can manipulate gene functions in vivo (e.g., opto-genetics) have enabled scientists to delve into the chemical and mechanical control of biological asymmetry across different scales, from molecules, to cells, to tissues, to organisms. By taking an inter-disciplinary approach that harnesses recent technologies from diverse fields of science and engineering, our laboratory will continue to pursue cutting-edge science and build a network with leading scientists in cell and developmental biology.
Proudly powered by Weebly